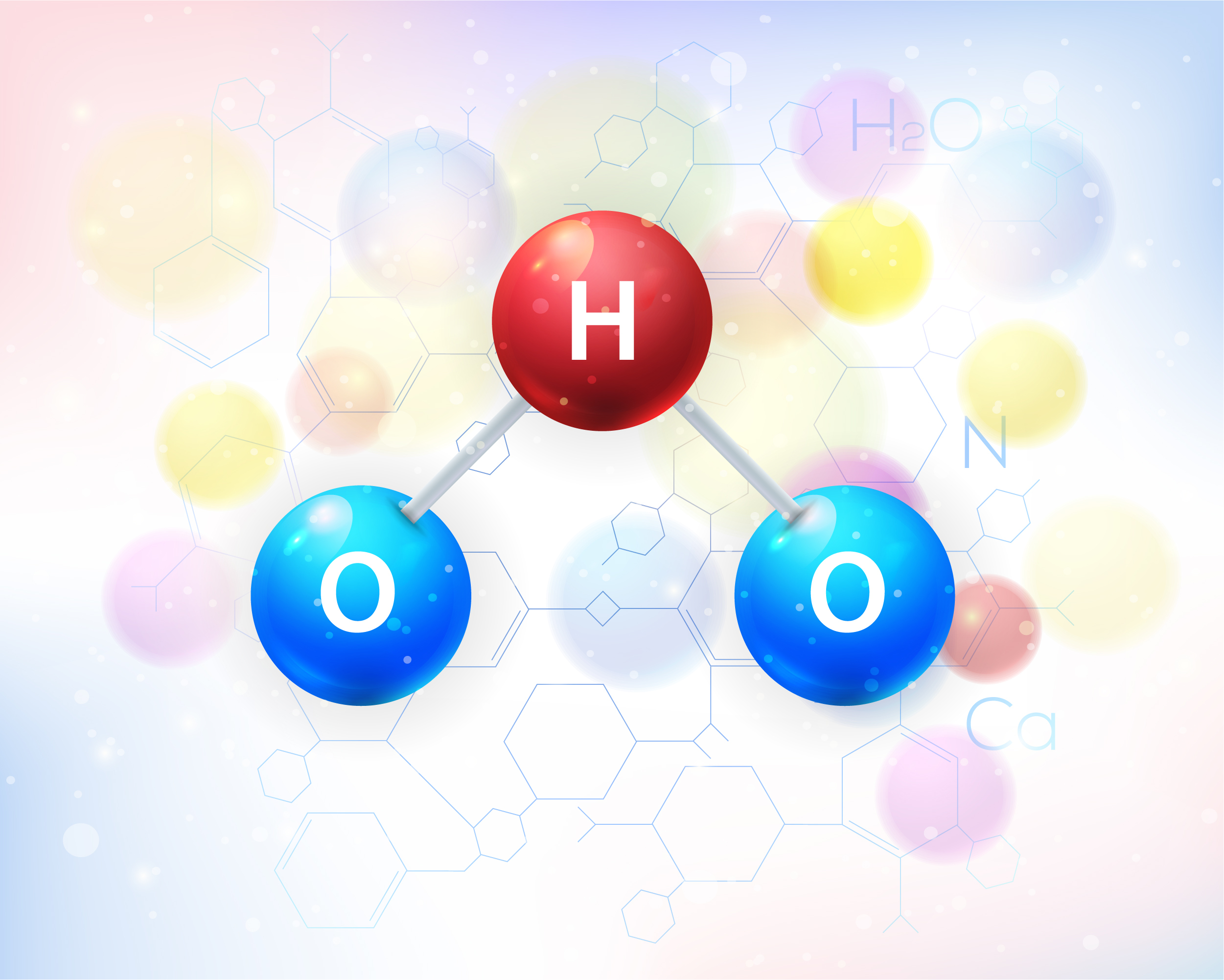
Er du i tvivl om, hvad der er polær og upolær molekyler, så kan du finde svaret her.
Lige nu læser andre
Det er ikke altid lige nemt at finde rundt i molekylernes verden, men her er lidt hjælp, hvis du sidder derude og har brug for at finde ud af, hvordan det ser ud med forskellen på polær og upolær i molekylernes univers.
Polær og upolær
Når nogle molekyler er positive i en ende og negative i den anden ende, kaldes de for polære.
Polære molekyler trækker i molekyler, der ligner dem selv, altså andre polære molekyler, fordi positiv og negativ tiltrækker hinanden.
Den negative ende vil altså gerne binde sig sammen med andre molekylers positive ende.
Læs også
Men der findes også molekyler, der hverken har en positiv eller negativ ende. Disse kaldes upolære.
Nu ved du, hvad der ligger i begreberne polær og upolær, og så er det tid til at sætte et eksempel på.
Polære molekyler
Vandmolekylet er som sagt polært og det kaldes også for en dipol, fordi den er i overskud, når det kommer til negative ioner i den ene ende, men samtidigt har et underskud af negative ioner i den anden.
Man taler om at vand har en ikke-symmetrisk elektronsky.
De polære stoffer, der kan blandes med vand kaldes hydrofile.
I vores eksempel med vand, indeholder det mange O og H-molekyler, som ofte er vandopløselige altså polære.
Upolære molekyler
Ved de upolære taler man om en symmetrisk fordeling af ladning. Disse er ikke vandopløselige. Molekyler der indeholder C-og H-atomer er oftest upolære.
De upolære stoffer, der altså ikke er blandbare med vand kaldes hydrofobe.
Molekylers opførsel
Molekyler er ved lav temperatur et fast gitter, fordi der her opstår dipoler, og dermed dannes der en usymmetrisk struktur.
Som vi tidligere var inde på, så betyder det ofte at de kan tiltrække andre molekyler.
Hvor dygtige de er til det afhænger af, hvilken størrelse de har, og her betyder en stor størrelse noget.
Det er nemlig sådan, at jo større og mere udstrakte molekylerne opbygning er, jo stærkere er deres tiltrækningskræft.
Den molekylære videnskab er som sagt ikke den nemmeste at gå til, og derfor kan det som sagt være en fordel at opsøge køkkenet og madlavning for at lære, hvordan de opfører sig, men nu ved du i det mindst, hvad polær og upolær indebærer.
Poplær og upolær i køkkenet
Et rigtig godt sted at studere molekyler og deres egenskaber og opførsel er faktisk i køkkenet.
Et godt eksempel på et polært molekyle er ganske almindeligt vand fra hanen.
Et godt eksempel på et upolært molekyle er til gengæld ganske almindelig olie til madlavning.
Når du forsøger at blande polær og upolær (her vand og olie), vil du opdage at de ikke kan blandes.
I hvert fald ikke uden hjælp fra en emulgator. Så det kan altså lade sig gøre, men de kan altså ikke i sig selv blandes og har så at sige behov for hjælp udefra for at kunne komme til at udføre en sådan handling.